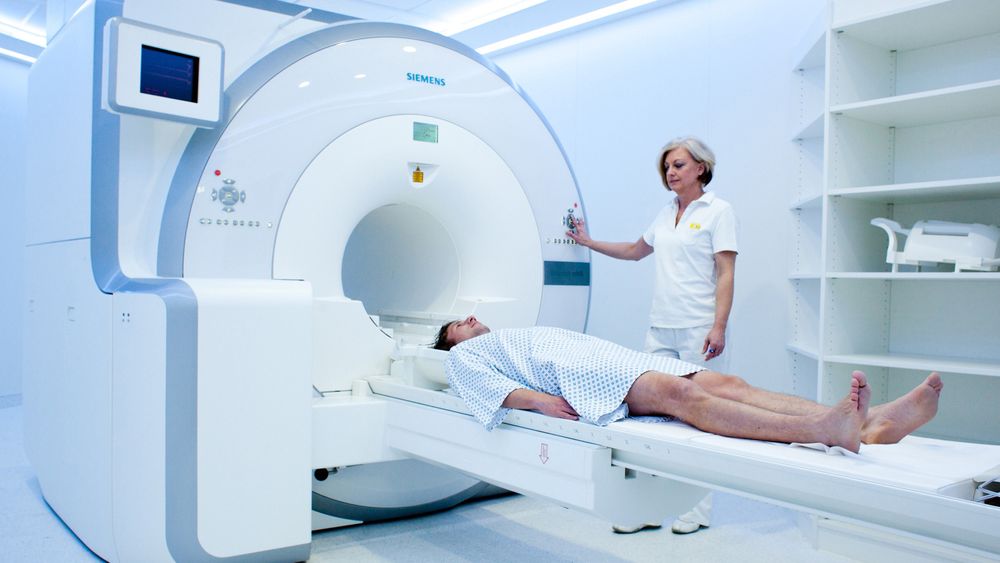
Det gode gamle røntgenapparatet, som ennå er selve grunnstammen i kroppsavbilding, har fått konkurranse.
Utviklingen har kommet som et resultat av nye ideer, ny teknologi og digitalisering. Det analoge har måttet vike for det digitale også på dette området.
Jo lenger inn mot detektoren ingeniørene har flyttet digitaliseringen, jo mindre har støyen hatt å si.
Spesielt i MR er det viktig å redusere signal-støyforholdet. For noen år siden var kabelføringen mellom 5 og 10 meter fra sensor til AD-en (analog til digitalomvandleren). I dag er det snakk om noen millimeter.
- Nå starter jakten: Har funnet en mal for å identifisere genene som gjør oss syke
MR - Magnetisk Resonans
MR, eller MRI (Imaging), har gått fra dyrt og avansert, til rimelig og standardisert på sykehus i løpet av de siste 30 årene.
Mens røntgen er best på skjelettdeler, og mindre bra på det bløte vevet, er det omvendt på MR. De to teknikkene utfyller hverandre effektivt.
En av de viktige grunnene til at vi har fått MR-maskiner var utviklingen av det som kalles Fast Fourier Transform som begynte på 60-tallet. FFT er algoritmer som raskt behandler signaler fra ulike sensorer, slik som de vi finner i medisinske billeddannende instrumenter. Og mye annet.
Det er den samme teknikken vi finner igjen i alt fra komprimert lyd, jpg-bilder og mpeg-video.


Supermagneter
Prinsippet bak MR er enkelt. På samme måte som i en CT-maskin, legges pasienten inn i noe som minner om en stor smultring.
Men den inneholder noe helt annet enn i CT-en. Inne i ringen finner vi en enormt kraftig elektromagnet som - for diagnostisk bruk - har feltstyrker på 1,5 tesla eller 3,0 tesla.
Magnetfeltet er så kraftig at hydrogenkjerner, det vil si protonkjernene i vannmolekylene, retter inn spinnretningen langs magnetfeltet.
Dette er utgangspunktet for å kunne skape bilder, men for å gjøre det må det komme informasjon strålende tilbake til sensorene. For å få noe tilbake som kan indikere hvordan vann er fordelt i vevet, sendes det inn en puls med et radiosignal sammen med magnetfeltet.
Når denne radiopulsen skrus av, dreier protonene tilbake til magnetfeltets retning og sender ut et ørlite radiosignal. Jo flere vannmolekyler i vevet, jo flere protonkjerner er det og desto sterkere blir signalet.


Fordi ulike organer inneholder ulike mengder vann, vil radiobølgene inneholde informasjon om dette. Men et spekter av radiosignaler er ikke spesielt betraktningsvennlig, og det er her FFT kommer inn for å produsere bildene.
Akkurat som i en CT-maskin tas det en rekke projeksjoner etter hverandre slik at det kan beregnes hvordan vannet fordeler seg i et volum. Derfra kan det skapes todimensjonale bilder i form av ulike snitt gjennom volumet.
MR er på langt nær et ferdig utviklet prinsipp. Utviklingen har vært drevet i stor grad av behovet for raskere opptak. Alle som har hatt en MR-undersøkelse, vet at dette tar tid. Nå har vi fått høyere oppløsning og etter hvert opptak av video.

Nord-Amerikas nye grensebru koster 51 milliarder kroner
Kraftigere feltstyrke
Til nå har de fleste slike maskiner typisk vært på 1,5 tesla (15.000 gauss), men trenden går nå mot kraftigere 3 tesla-maskiner. I Norge er rundt 20 prosent av MR-maskinene nå på 3 tesla og et økende antall av de MR-systemer som anskaffes i dag er 3.0 tesla-systemer.
Den høyere feltstyrken gir enda bedre innblikk i bløtvevet gjennom økt signal-støyforhold og litt høyere oppløsning, men er ikke uten utfordringer:
Nerver, blodårer og andre typer vev leder strøm forskjellig, og i tillegg vil overgangen mellom slike ledere og det isolerende vevet rundt gjøre det vanskeligere å ta bilder.
Derfor har moderne 3.0 tesla MR-maskiner to radiosendere i stedet for en, og utviklingen går mot enda flere. Med to eller flere RF-sendere og avanserte radiopulser kan man eliminere disse forhold og forme radiopulsene for å utligne pasienters ulike egenskaper og form.
For å skape de de kraftige magnetfeltene krever elektromagnetene enorme strømstyrker. Dette oppnås med magnetspoler med superledere, som blir superkjølt til flytende helium ned til 4,2 grader kelvin. Dette er kokepunktet for flytende helium.
Bedre spoler
Antennene som fanger opp signalene fra pasienten kalles - i MR-terminologi - for spoler eller coils, og disse har gjennomgått en stor utvikling.
De er utformet med nye og bedre materialer, og man bygger nå flere spoleelementer inn i den samme spolen. Det har gjort det mulig å gjøre parallelle opptak. Flere spoleelementer i en antenne på pasienten gir raskere opptak.
Det har også gitt MR-maskinene bedre oppløsning og bedre bildekvalitet. I tillegg har man kunnet realisere dynamiske opptak, fordi man har fått et tilstrekkelig antall bilder i sekundet til å se bevegelser.
- På fjellet i påsken? Denne varsler når du må bort fra solen
Kvantifisering
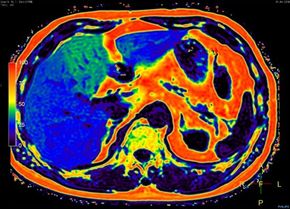
I dag brukes primært MR til å lage bilder, men teknologien kan også gjøre andre ting, slik som å måle temperaturen svært presist inne i kroppen.
Den kan også brukes til å måle andre kvantifiserbare verdier inne i kroppen, som for eksempel hvor mye blod det flyter i en åre, hvor mye fett det er i leveren, hvordan fordelingen av ulike typer fett er, hvor mye jern det er i vevet og hva effekten av ulike medisiner er på forskjellige organer.
Det siste kan være svært viktig informasjon når man skal si noe om hvordan en tumor responderer på behandling.
Fysikken i en MR-maskin er godt forstått, men det er fremdeles en del å gå på ved å bruke stadig mer presis forståelse av fysikken på den ene siden og kroppen på den andre. En slik trend er å benytte preparater for å få bedre bilder av enkeltorganer.

Tre tiltak kan gi oss utslippsfri tungtransport
Hybride MR-maskiner
Hybrid-MR er en kombinasjon av en MR-maskin og utstyr som kan behandle pasienten.
Med slikt utstyr kan legen se resultatet av behandlingen i sanntid. Man kan for eksempel benytte MR-bilder til å styre en rekke ultralydsendere som varmer opp kreftvev for å drepe det.
Dette krever ekstrem nøyaktighet når det gjelder både posisjon og kontroll av temperatur i det volumet som varmes opp. MR kan også brukes til å overvåke en kreftsvulst som skal behandles medikamentelt.
Cellegift pakket inn i ørsmå partikler i beskyttende fett kan «pakkes ut» med ultralyd ved å øke temperaturen lokalt fra 37 til 42 grader når medisinen kommer frem.
På den måten kan et medikament frigjøres kun der det skal ha virkning: Dosen kan mangedobles og virkningen forbedres.
En annen hybrid teknologi er å bruke MR til å styre strålebehandling av kreft; en MR-lineærakselerator.
En slik teknologi, som består av en strålemaskin og en MR-maskin bygget sammen til en, utvikles i et samarbeid mellom Elekta i Storbritannia og Philips i Finland. Den må løse to motstridende utfordringer:
En MR er svært følsom for metall i en lineærakselerator for magnetfelt. Løsningen er å bygge maskinen svært symmetrisk og ha en aktiv skjerming mot både radiobølger og magnetfelt.
Med en slik maskin er det mulig å bestråle svulster i organer som beveger seg, slik som lunger og tarmer, eller en prostata som alltid er i en viss bevegelse.
En slik såkalt MR-Linac-maskin, vil gi en bedre, målrettet, strålebehandling i visse anatomiområder og skåne omliggende vev. Hybridteknologien er bare i starten og flere ulike varianter vil komme.
CT Computer Tomography
Computer Tomography (CT) krever, akkurat som MR-teknologien, betydelig datakraft. Den setter også sammen et bilde på grunnlag av en serie gjennomlysninger av kroppen.
En CT-maskin er utformet som en smultring, der pasienten ligger på en benk inne i hullet. I ringen rundt er det en røntgenkilde på den ene siden og en røntgendetektor på den andre siden.
Begge roterer sammen og tar typisk fra 32 til 256 ulike snittbilder av kroppen som ligger på benken.
Med så mange bilder kan datamaskinen, ut fra differansene, regne ut et tredimensjonalt bilde av det belyste kroppsvolumet.
Ut fra det kan man beregne nye bilder som beskriver ulike snitt gjennom kroppen. Altså omtrent som om både røntgenkilden og sensoren hadde vært montert inne i kroppen.
CT med gråtoner
Digitaliseringen av røntgen (og CT) har gitt store gevinster. Ved å belyse kroppsdeler i ulike spekter kan man få mer informasjon.
Utviklingen er i ferd med å gå fra en og to spektre til multispektrale maskiner. En multispektral CT-maskin vil ha bueformede sensorer i en viss bredde.
Sensorene består av mange sjikt med ulik følsomhet for røntgenstråler i ulike frekvensbånd. På den måten får man representert vevet i gråtoner i stedet for sort-hvitt, og kan se langt flere detaljer.
Denne utviklingen gjør at langt billigere og raskere CT-maskiner på flere områder kan erstatte MR-maskiner, fordi de har mye bedre oppløsning på bløtt vev enn tradisjonell CT.
- Les også: Slik utføres en grå stær-operasjon
PET
Positronemisjonstomografi (PET) er en ny og kostbar teknologi for å finne svulster i kroppen. Tomografen ser ut som den vi finner i MR og CT ved at kroppen ligger inne i en «smultring». Men detektorene i en PET er beregnet på å fange opp fotonstråling som kommer fra kroppen.
Da må det injiseres et radioaktivt kontrastmiddel i kroppen. Slike kontrastmidler, som isotoper av karbonoksygen, må lages på stedet fordi de har en halveringstid på typisk 1,5 timer eller mindre (oksygen kan også benyttes, men er i særstilling med en halveringstid på ca. 90 sekunder).
Derfor må det i umiddelbar nærhet finnes en syklotron som kan produsere slike isotoper.
Isotopen pakkes inn i sukker og injiseres i blodet. Svulster er svært energikrevende og vil vises på bildene, fordi de absorberer mye mer av sukkeret enn vevet rundt.
Selve tomografen har en eller flere detektorer som registrerer fotoner som produseres når isotopen henfaller. Forskjellen i tid bestemmer posisjonen til isotopen, og mengden fotoner forteller hva som er vev og hva som er svulst.
En PET-maskin kan ha en følsomhet på svulster som er 10.000 til 100.000 ganger bedre enn en MR-maskin. Slike maskiner er også veldig godt egnet til å oppdage om kreften har spredt seg.
PET-teknologien er i rask utvikling, ikke minst på isotopsiden. Andre typer isotoper kan gi mer informasjon om svulstene enn det vi får i dag.
Det finnes fem PET-maskiner i Norge. På grunn av kravet til lokal produksjon av isotoper og logistikken rundt er dette svært kostbare installasjoner.
- Les også: Googles nye Android skal være overalt

Politikken kutter EUs behov for gass – ikke varmere vær eller krig
MPI
Magnetic Particle Imaging (MPI) er en ny teknologi som benytter nanopartiker av jernoksid i en kontrastvæske.
Selve tomografen består av en serie elektromagneter rundt pasienten. De registrerer de mikroskopiske endringene i magnetfeltet som oppstår når partiklene beveger seg gjennom kroppen.
Det gir informasjon om partiklenes konsentrasjon og posisjon. MPI kan gi bedre innsikt i pasientens biokjemi uten bruk av isotoper, og man tror teknologien kan fylle et hull mellom MR og PET. Teknologien er ikke tatt i bruk for mennesker ennå.
Ultralyd
Utviklingen i ultralyd er minst like rask og spennende som disse maskinene, men den har vi dekket i denne artikkelen.
- 400 millioner mennesker trenger en slik: Nå kommer en norsk revolusjon
Programvare
MR, CT og PET er tung maskinvare som gir fra seg en voldsom strøm av data som må regnes om til bilder. Derfor er programvaren som gjør denne jobben svært viktig.
Ny programvare kan nå sette sammen slike bilder svært mye raskere enn før. Det som tok et par timer for bare to år siden, kan nå gjøres unna på et par minutter, og man kan få et midlertidig bilde i sanntid.
Nye støttesystemer for diagnostikk og terapi basert på maskinlærende kunstig intelligens er det store forventninger til.
IBMs Watson datasystem er allerede «i jobb» som legeassistent på mange sykehus i USA og gir behandlende lege forslag på basis av enorme mengder medisinsk informasjon og pasientenes egne data.
Hjemmediagnose
Alskens dyre instrumenter på sykehus kan snart bli utfordret av billige sensorer vi bærer på oss til enhver tid, eller som vi har i hjemmet.
Alt fra smartklokker som logger kontinuerlig puls til madrasser som måler fettvev, svetting og andre parametre kan gi indikasjoner på sykdom måneder og år før vi oppdager det på annen måte.
Slikt utstyr er billig, og folk vil anskaffe det for egen regning. Utfordringen er hvem som skal samle data og analysere dem for sykdomstegn. Skal det være Google, Apple eller helsevesenet?
Kilder: Øystein Brenne, produktsjef MR Philips Nordic, og Jørn Kværness, MR clinical scientist Philips Nordic.

Beyonder: – Et norsk produkt produsert i Kina