Forskere i Aarhus i Danmark gjør seg klare til å redigere gener i stamceller fra pasienter med medfødte defekter i immunsystemet. Målet er kliniske tester om få år.
Nå settes det i gang et stort prosjekt i Aarhus med sikte på å gen-redigere seg ut av problemer med immunforsvaret, noe som i dag er potensielt dødelig for noen.
– Vi er ute etter å finne metoder som gjør at man kan rette opp defekten i pasientens egne celler, slik at risikoen i forbindelse med vanlige behandlinger er minimert, og virkningen er livslang, forteller Trine H. Mogensen.


Hun er avdelingslege og professor på Infektionsmedicinsk avdeling og Institut for Biomedicin og Institut for Klinisk Medicin ved Aarhus Universitetshospital.
Alvorlige problemer i immunsystemet har blant annet den konsekvensen at pasientene kan dø av ellers harmløse mikroorganismer som vi daglig blir overøst med fra naturens side.
I det femårige prosjektet som har fått 25 millioner kroner i støtte fra den danske Innovationsfonden, blir fokus primært satt på pasienter med sjeldne immundefekter, så som SCID (alvorlig kombinert immundefekt), som er svært alvorlige, men som bare rammer omkring ett av 100.000 mennesker.
Dødelige sykdommer uten behandling
Denne typen sykdommer er nedarvet, og er derfor til stede helt fra fødselen, hvor barna ofte må skjermes fullstendig fra omverdenen for ikke å pådra seg et potensielt dødelig virus eller en bakterie som kan forårsake lungebetennelse, blodforgiftning eller vannkopper.
Problemet er at en genfeil eller en kombinasjon av flere feil, fjerner muligheten som de hvite blodlegemene har til å avhjelpe inntrengningen av mikroorganismer. Men ved å bruke gensaksen Crispr/Cas9 håper man at de problematiske mutasjonene i genene kan redigeres ut av cellene, og altså erstattes med friske gener.
For å komme så langt, må Crispr/Cas9 klippe over DNA-et på det stedet hvor den alvorlige mutasjonen ligger. Ved å legge inn et brudd i DNA-et tvinges cellen til å reparere det ødelagte DNA-et. Og nettopp den prosessen gjør det mulig å sette inn ny genetisk informasjon og reparere mutasjonen nær bruddstedet.
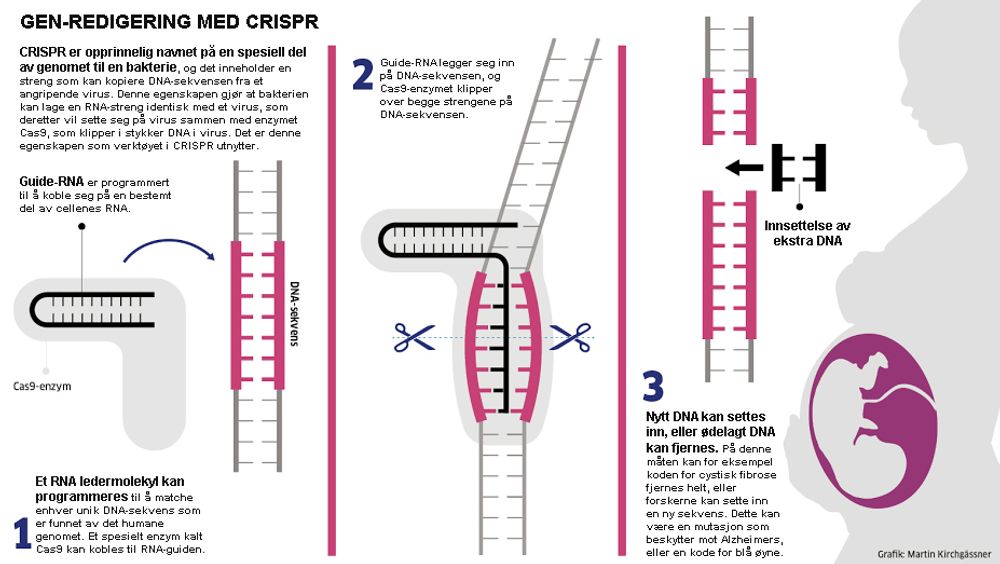
Slik fungerer Crispr/Cas9
- Crispr er opprinnelig navnet på en spesiell del av genomet til en bakterie, som inneholder en streng som kan kopiere DNA-sekvensen fra et angripende virus.
- Den egenskapen gjør at bakterien kan skape en RNA-streng identisk med virus, som deretter kan sette seg på virus sammen med enzymet Cas9, som klipper i stykker DNA i virus. Det er denne egenskapen som verktøyet Crispr utnytter.
Cellene må deretter formeres opp, og settes inn i pasienten igjen i håp om at de vil overleve og gi opphav til normalt fungerende blodceller. Og i tillegg, i noen tilfeller, utkonkurrere de syke cellene.
Rent metodisk skal forskerne samle opp stamceller fra en rekke pasienter med disse sykdommene. De blir tatt ut fra blod eller beinmarg, og gjøres klar til behandling med Crispr/Cas9-saksen. Den består av to komponenter: Et protein (Cas9), som skal klippe i DNA-et, og et lite leder-molekyl som styrer saksen til det rette stedet i arvemassen.
Sikrere enn beinmargstransplantasjon
De to komponentene bringes inn i pasientens celler ved å gi dem et lite elektrosjokk som bringer saksen helt inn i cellekjernen.
Forskere rundt om i hele verden jobber med å avhjelpe sjeldne, arvelige sykdommer ved hjelp av denne metoden, men foreløpig gjøres det meste av arbeidet i laboratoriene. Målet er nå å ta et stort skritt framover mot klinisk prøving og bruk ved å arbeide videre på eksisterende forskning.
Blant annet er teknikken med å redigere stamceller og la dem overta territoriet i immunforsvaret over de syke cellene, testet ut i mus på en rekke andre gen-sykdommer. Det har sett ut til å fungere, og kliniske tester av andre gen-rettelser har også vist seg å være positive. Men ellers finnes det ikke mye erfaring, forteller Trine H. Mogensen, som i dette prosjektet blant annet står for å få gjennomført helgenom-sekvenseringer av både nyfødte og voksne som viser tegn på immundefekter, inkludert SCID.
– Vi har foreløpig 10–20 pasienter som vi kan prøve å behandle, men målet er også å diagnostisere og finne flere pasienter i løpet av disse fem årene, siden man ofte trenger behandling tidlig i løpet av de første leveårene, understreker Trine H. Mogensen.


– Vi mener også at denne metoden er mye sikrere enn for eksempel beinmargstransplantasjon, som man benytter i dag. Ved den typen behandling må man sette friske celler fra pasienten selv eller en passende donor inn i kroppen, noe som innebærer at man først helt må ødelegge resten av sitt eget immunforsvar med kjemoterapi for å bygge opp det nye. Og det er en veldig risikabel prosess som vi forhåpentlig snart kan slippe, sier hun.
- DNA-teknologien fjerner syke gener: Her kan kuren for HIV og kreft ligge
Fremdeles en del utfordringer
Men det finnes en del utfordringer som må overvinnes først. For det første skal Crispr/Cas9-systemet ledes fram til det rette stedet.
Og selv om det etter hvert har blitt opparbeidet stor erfaring i bruken av gensaksen blant forskere, dreier det seg ikke her bare om å få den til å foreta et klipp i DNA-strengen, men om at det blir gjort så presist at man også er sikker på at saksen ikke har klart å gjøre andre endringer i arvemassen, noe som på sikt kan føre til bivirkninger som kreft. Det er en av de spesielt fryktede scenariene ved bruk av Crispr/Cas9.
Men selv her er den vanskeligste delen ikke foretatt ennå, forteller genforsker og professor på Institut for Biomedicin Jacob Giehm Mikkelsen, som også deltar i prosjektet.
– Det vanskeligste er faktisk å korrigere mutasjonen ved å tilby en bit DNA som cellen kan bruke som sjablong til å stenge hullet. Det er viktig at sjablongen fungerer effektivt i cellen, for ellers vil cellen selv stenge hullet i DNA-et ved å lime sammen de to løse endene, ofte med en ny mutasjon til følge, forklarer han.
– Sjablongen vår ligner DNA-et i det aktuelle området – selvfølgelig nær mutasjonen – og den kan cellen benytte når hullet lappes, sier Jacob Giehm Mikkelsen.
- Kan bli tiårets mest nyttige eller mest skadelige forsøk: Genmodifisering skal utslette malariamygg
Timing er avgjørende
Timingen er viktig i denne forbindelsen, for sjablongen skal helst være til rådighet i det øyeblikket da saksen klipper, og derfor overveier forskerne om sjablongen helst må føres inn dagen før saksen tas i bruk.
Men selv når det rette klippet har blitt gjort, og en frisk streng satt inn, må det også fungere når pasientene deretter får cellene tilbake.
Ifølge Trine H. Mogensen har museforsøk tidligere vist seg effektive.
– Det finnes også noen ganske lovende prosjekter på verdensbasis. Blant annet et prosjekt med gensykdommen sigdcelleanemi (som forårsaker lav blodprosent, red.), hvor det har lyktes veldig godt å korrigere genfeilen. Det er en enklere sykdom, men vi håper å kunne få til det samme, sier Trine H. Mogensen.
Flere prosjekter i gang
Forskergruppen jobber parallelt på flere prosjekter. Et annet handler om å skape miniversjoner av hele, friske gener og sette dem direkte inn i pasientens stamceller med den hensikten å utbedre genfeilen og samtidig sette det syke genet ut av spill. På den måten slipper man redigeringsarbeidet, og trenger bare å sette inn et helt nytt gen på den riktige posisjonen i arvemassen.
– En slik strategi, som innebærer at det gamle genet så å si dyttes til side, kan man bruke bredere, for kanskje ti eller flere forskjellige mutasjoner i ulike pasienter. Problemet er nemlig at Crispr/Cas9-behandlingen ellers må utvikles helt spesifikt for den enkelte pasienten. Det kan bli en utfordring når nye pasienter med nye mutasjoner dukker opp, sier Jacob Giehm Mikkelsen.
– Men vi vil hele tiden være på jakt etter nye mutasjoner og muligheten for å målrette den genetiske behandlingen til den enkelte pasienten. Dette er i høy grad personlig medisin, men med disse metodene kan vi forhåpentlig bli raskere, sier han.
Med i prosjektet er også Institut for Klinisk Medicin, Afdeling for klinisk immunologi og Aarhus Institute for Advanced Studies. Alle er underlagt Aarhus Universitet.
Artikkelen ble først publisert på Ing.dk
- 5 tips fra eksperten: Slik bruker du LinkedIn for å få gode teknologi-jobber (TU Ekstra)