Tekst: Knut Erik Boland, Inline Prosess


Artikkelen dekker blant annet på målemetoder, temperaturpåvirkninger samt kalibrering og vedlikehold, for pålitelige resultater.
Trenger kompensering
Ledningsevnemåling er en rimelig og rask måte å måle ionestyrken i en væske på. Dog med den begrensningen at målingen ikke er 100 % spesifikk eller selektiv, se saken ”Spesialmålinger” på høyre side.
Partikler i væsken, uten ladning og innhold av for eksempel organiske alkoholer eller sukker, vil ikke gi bidrag til ledningsevnen. Temperaturen og temperaturforandringer påvirker også ledningsevnen, da dette påvirker molekylenes/ionenes evne til å binde eller løsrive seg, og også mobiliteten til ionene. Se kompensering senere i artikkelen.
Les også: Slik fungerer turbiditetsmålingen
Proporsjonalt med strømstyrken
Elektrisitet er en flyt (engelsk: ”flow”) av elektroner. Dette indikerer at ladde partikler vil lede elektrisitet. Konduktivitet er evnen til en væske å lede elektrisk strøm. Ut fra dette, er det naturlig at strømstyrken som oppnås, er proporsjonal med antall ioner i væsken. Måling av en væskes ledningsevne er således en direkte avlesing av ionekonsentrasjonen i væsken.
Alle væsker har en viss ledningsevne. Selv i ultrarent vann som benyttes i eksempel farmasøytisk industri og elektronikkindustrien, kan ledningsevnen måles meget nøyaktig. I andre enden av skalaen finner vi applikasjoner i kjemisk industri, hvor man gjerne måler på syrer og baser, i galvaniske bad og sterke saltløsninger som eksempler.
Spesifikk konduktivitet
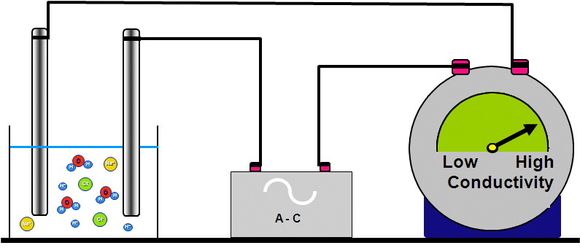
Historisk ble ledningsevne- eller konduktivitetsmåling målt mellom 2 platinaplater. Størrelsen var 1 cm x 1 cm, og de var plassert med 1 cm avstand fra hverandre. Dette oppsettet, med eksakte mål, forenklet i begynnelsen ”forskningen” av måleresultatene og hvordan platinaplatene ble påvirket underveis, med tanke på polariseringseffekter, på overflaten, og dertil reduksjon av målecellens prestasjoner.
Dette var også en kostbar og skjør målecelle å produsere, men ga verdifulle resultater. Dessuten kom vi frem til formelen for spesifikk konduktivitet, C, som tar hensyn til elektrodens geometri.
Kunduktans
Fordi ledningsevneverdier blir påvirket av målecellens geometri, skulle uttrykket spesifikk ledningsevne, C, komme til anvendelse. Hvis målecellen senkes ned i en væske med konduktans, G, vil ledningsevnen, mellom elektrodene (platene), bli følgende uttrykk:
C = G x L /A
.png)

Hvor C = konduktivitet i Siemens / cm (S/cm)
G = konduktans i Siemens (1/R, inverse av ohm)
L = avstanden mellom elektrodene (cm)
A = arealet av elektrodene (cm2)
Cellekonstant
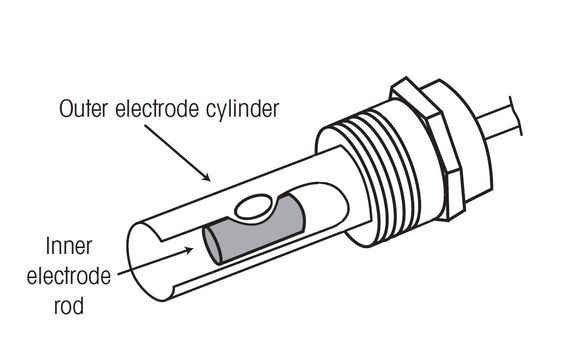
Uttrykket L/A i ligningen over, betegnes som sensorens cellekonstant. I en tradisjonell ledningsevnesensor, med areal 1 cm2 på elektrodene og 1 cm avstand mellom dem, får vi cellekonstant lik 1.00 cm-1. Med denne geometrien, eller avstanden mellom elektrodene, gir dette et temmelig stort måleområde, fra typisk 1 µS/cm opptil 100 mS/cm. Ønsker man å måle på destillert eller ultrarent vann, med ledningsevne godt under 1 µS/cm, benyttes en sensor med cellekonstant 0,1 eller 0,01 cm-1, hvor avstanden mellom elektrodene (platene) er redusert (minsker L). Tilsvarende når det gjelder å måle på væsker med høy ledningsevne, kan avstanden L økes for å gi en større cellekonstant, for eksempel 10 cm-1.
Les også: Automatiserings innsiktsartikkel om pH-målling
2-elektrodesensoren
Sensoren beskrevet ovenfor, er en såkalt 2-elektrodesensor. Som navnet tilsier, har den 2 elektroder (plater). Denne sensoren har sin styrke i væsker med lav ledningsevne. Men den er følsom for beleggdannelse på elektrodene. Og bør derfor rengjøres jevnlig.
Beleggdannelse vil selvsagt påvirke sensorens målenøyaktighet. I tillegg kan det også gi uønskede polariseringseffekter, hvis belegget består av ladde partikler eller ioner. Man kan nærmest få en ”kondensatorvirkning” på overflaten av elektrodene mot belegget. Dette igjen ”blokkerer” elektrodenes mulighet til å måle på de andre, frie ionene i vannet, mellom elektrodene (platene).
4-elektrodesensoren
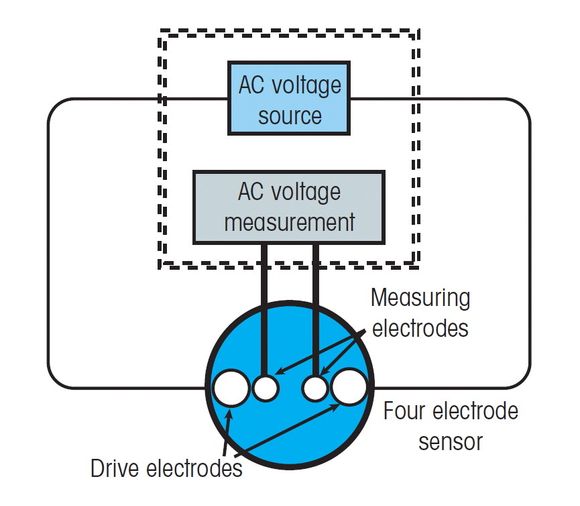
En 4-elektrode sensor kan være et bedre valg. Her påtrykkes en vekselspenning de to ytre elektrodene, og avhengig av ioneaktiviteten, vil det dannes en tilsvarende strømstyrke som fanges opp i de to indre elektrodene. Strømstyrken er proporsjonal med ionestyrken/-aktiviteten i væsken.
Dette er de viktigste fordelene med 4-elektrodeprinsippet sammenlignet med 2-elektrodesensoren:
- Mindre følsom for beleggdannelse.
- Små eller ingen polariseringseffekter
- Større måleområde
Begrensninger:
- Ikke så nøyaktig på lave måleområder
- Kan ikke måle på destillert/ultrarent vann.
Induktiv måler
I tillegg til 2- og 4-elektrode sensor måleprinsipp, har vi induktivt måleprinsipp. Sensoren fungerer som en transformator, med 2 spoler montert ved siden av hverandre. Den ene spolen påtrykkes en spenning. På grunn av ledningsevnen i målevæsken, vil det bli indusert en spenning i den andre spolen. Og denne er proporsjonal med ledningsevnen i vannet.
Fordelene, med en induktiv ledningsevnesensor, kan oppsummeres slik:
- Helt ”hermetisk”. Kun et materiale er i kontakt med prosessvæsken.
- Stort måleområde <= 2000 mS/cm.
- Ingen polariseringsproblematikk.
- Meget solid, tåler krevende prosesser.
- Minimalt vedlikehold.
Temperaturkompensering

I likhet med de fleste prosessmålinger, påvirker temperaturen måleresultatene. Et referansepunkt er derfor nødvendig; Normalt 25 grader C. Temperaturkompensering kan gjøres automatisk i måleren, med typisk koeffisient 1-3 % per grad C. Standardkompensasjon er gjerne satt til 2,1 %/grad C, men den kan justeres, for å tilpasses væskens spesifikke temperaturkoeffisient.
For visse væsker, for eksempel ultrarent vann, er temperaturendringene ulineære. Målerne kan derfor ha spesielle algoritmer for en bedre temperaturkompenasjon.
Temperaturen påvirker ledningsevnen i væsken hovedsakelig på to måter:
- Dannelse av flere ioner med økende temperatur (komponenter går over til ioneform).
- Mobiliteten, til ionene øker, med økende temperatur.
Ut ifra dette ser vi at ledningsevnen øker med økende temperatur, og vice verca.
| Stoff/substans ved 25 grader C | Konsentrasjon i % | Temperaturkoeffisient |
| HCL | 10 | 1,56 |
| KCL | 10 | 1,88 |
| NaCL | 10 | 2,14 |
| HF | 1,5 | 7,20 |
| Ultrarent vann | N/A | 5,00 |
Noen eksempler på stoffer og deres temperaturkoeffisienter
Kalibrering
Benytt alltid frisk standard kalibreringsløsning, for eksempel 1413 µS/cm (20 grader C). Rengjør sensoren grundig, for eventuelt belegg, før kalibreringen starter. Det som skjer, ved kalibrering, er rett og slett en justering av cellekonstanten.
Hvor ofte skal det kalibreres? Det bestemmes ut ifra belastning, fysisk og kjemisk, og krav om målenøyaktighet. Som et minimum bør systemet sjekkes 1 gang/måned.
Rengjøring
Likt løser likt i kjemien. Men ut ifra et miljøhensyn, er ofte varmt vann + kraftig husholdingssåpe godt nok. Sensorene kan lagres tørt.







